Биохимия
Строение и свойства пептидной связи
Аминокислоты способны соединяться между собой связями, которые называются пептидными, при этом образуется полимерная молекула.
Пептидная связь – это связь между альфа-карбоксильной группой одной аминокислоты и альфа-аминогруппой другой аминокислоты.
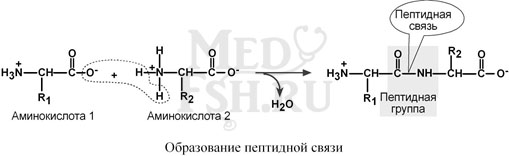
При необходимости назвать пептид ко всем названиям аминокислот добавляют суф- фикс «-ил», только последняя аминокислота сохраняет свое название неизменным.
Например, аланил-серил-триптофан или гамма-глутаминил-цистеинил-глицин (по-другому называемый глутатион).
К свойствам пептидной связи относятся:
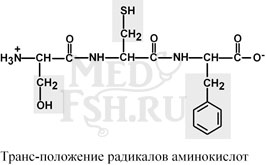
1. Трансположение заместителей (радикалов) аминокислот по отношению к C-N связи.
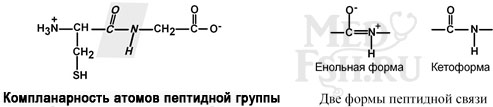
2. Компланарность
Все атомы, входящие в пептидную группу, находятся в одной плоскости, при этом атомы «Н» и «О» расположены по разные стороны от пептидной связи.
3. Наличие кетоформы и енольной формы.
4. Способность к образованию двух водородных связей. Атомы кислорода и водорода, входящие в пептидную группу, обладают способностью образовывать водородные связи с атомами кислорода и водорода других пептидных групп.
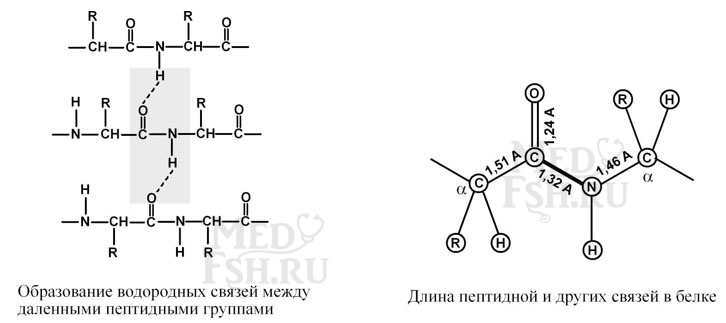
5. Пептидная связь имеет частично характер двойной связи. Ее длина меньше, чем одинарной связи, она является жесткой структурой, и вращение вокруг нее затруднено.
Но так как, кроме пептидной, в белке есть и другие связи, цепочка аминокислот способна вращаться вокруг основной оси, что придает белкам различную конформацию (пространственное расположение атомов).