Биохимия
Физико-химические свойства аминокислот
1. Являются амфотерными электролитами
Аминокислоты сочетают в себе свойства кислот и оснований. Соответственно, в водном растворе аминокислоты ведут себя как кислоты – доноры протонов и как основания – акцепторы протонов.
Если общий заряд аминокислоты равен 0, то это ее состояние называют изоэлектрическим. Величина рН, при которой заряд аминокислоты равен 0, называется изоэлектрической точкой (ИЭТ, pI). Значение изоэлектрической точки зависит от строения радикала аминокислоты:
- pI большинства аминокислот располагается в диапазоне рН от 5,5 (фенилаланин) до 6,3 (пролин),
- pI кислых аминокислот – рI глутамата 3,2, рI аспартата 2,8,
- pI основных аминокислот – pI гистидина 7,6, pI аргинина 10,8, pI лизина 9,7.
pI гистидина позволяет ему использоваться в гемоглобиновой буферной системе и в функции особых веществ миоцитов (карнозина, анзерина) в которых он содержится. Эти соединения легко принимают и легко отдают ионы водорода при малейших сдвигах рН среды (в норме 7,35-7,45).
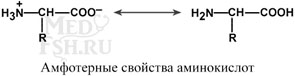
2. Заряд аминокислот зависит от величины рН среды
Отправным пунктом для понимания причин появления заряда у аминокислот является величина изоэлектрической точки (pI). Ситуация различается для нейтральных, кислых и основных аминокислот.