Биохимия
Ферментативный катализ
Основу всех жизненных процессов составляют тысячи химических реакций, катализируемых ферментами. Значение ферментов точно и образно определил И.П.Павлов, назвав их «возбудителями жизни». Нарушения в работе ферментов ведут к возникновению тяжелых заболеваний (фенилкетонурия, гликогенозы, галактоземия, тирозинемия) или существенному снижению качества жизни (дислипопротеинемии, гемофилии).
Известно, что для осуществления химической реакции необходимо, чтобы реагирующие вещества имели суммарную энергию выше, чем величина, называемая энергетическим барьером реакции. Для характеристики величины энергетического барьера Аррениус ввел понятие энергии активации. Преодоление энергии активации в химической реакции достигается либо увеличением энергии взаимодействующих молекул, например, нагреванием, облучением, повышением давления, либо снижением требуемых для реакции затрат энергии (т.е. энергии активации) при помощи катализаторов.
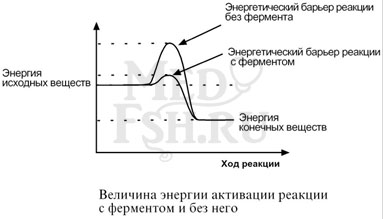
По своей функции ферменты являются биологическими катализаторами. Сущность действия ферментов, так же как неорганических катализаторов, заключается:
- в активации молекул реагирующих веществ,
- в разбиении реакции на несколько стадий, энергетический барьер каждой из которых ниже такового общей реакции.
Однако энергетически невозможные реакции ферменты катализировать не будут, они ускоряют только те реакции, которые могут идти в данных условиях.
Этапы ферментативного катализа
В ферментативной реакции можно выделить следующие этапы:
- Присоединение субстрата (S) к ферменту (E) с образованием фермент-субстратного комплекса (E-S).
- Преобразование фермент-субстратного комплекса в один или несколько переходных комплексов (E-X) за одну или несколько стадий.
- Превращение переходного комплекса в комплекс фермент-продукт (E-P).
- Отделение конечных продуктов от фермента.
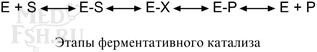
Механизмы катализа
1. Кислотно-основной катализ – в активном центре фермента находятся группы специфичных аминокислотных остатков, которые являются хорошими донорами или акцепторами протонов. Такие группы представляют собой мощные катализаторы многих органических реакций.

2. Ковалентный катализ – ферменты реагируют со своими субстратами, образуя при помощи ковалентных связей очень нестабильные фермент-субстратные комплексы, из которых в ходе внутримолекулярных перестроек образуются продукты реакции.
Типы ферментативных реакций
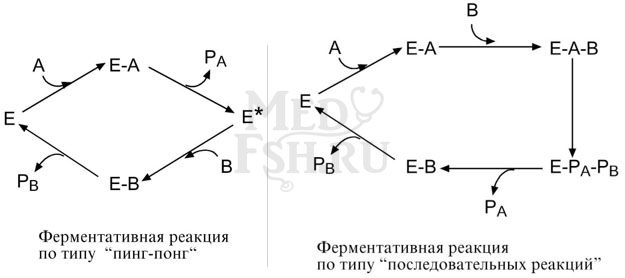
1. Тип «пинг-понг» – фермент сначала взаимодействует с субстратом А, отбирая у него какие-либо химические группы и превращая его в соответствующий продукт PA. Затем к ферменту присоединяется субстрат В, получающий эти химические группы. Примером являются реакции переноса аминогрупп от аминокислот на кетокислоты (см «Трансаминирование»).
2. Тип последовательных реакций – к ферменту последовательно присоединяются субстраты А и В, образуя «тройной комплекс», после чего осуществляется катализ. Продукты реакции PA и PB также последовательно отщепляются от фермента.
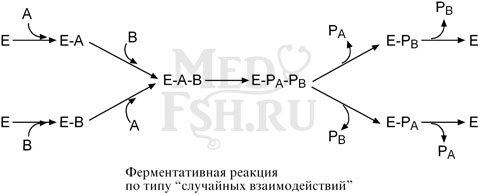
3. Тип случайных взаимодействий – субстраты А и В присоединяются к ферменту в любом порядке, неупорядоченно, и после катализа так же отщепляются.
Сходство и отличия ферментов и неорганических катализаторов
Сходство
- Катализируют только энергетически возможные реакции.
- Не изменяют направления реакции.
- Ускоряют наступление равновесия реакции, но не сдвигают его.
- Не расходуются в процессе реакции.
Отличия
- Скорость ферментативной реакции намного выше.
- Высокая специфичность.
- Мягкие условия работы (внутриклеточные).
- Возможность регулирования скорости реакции.
Скорость ферментативной реакции пропорциональна количеству фермента.