Антитела. Строение и функции иммуноглобулинов. Динамика антителообразования
Антитела – белки (гликопротеины) сыворотки крови, образующиеся в ответ на введение антигена и обладающие способностью специфически взаимодействовать с антигенами, которые вызвали их образование.
Функции антител в организме
- Взаимодействие с комплементарными структурами антигена с целью его нейтрализации и последующей элиминации.
- Обеспечение кооперации иммунокомпетентных клеток.
- Участвуют в различных защитных реакциях организма (активации комплемента, фагоцитозе – опсонизирующее действие, аллергии, иммунологической памяти и толерантности).
- Антитоксический эффект.
- Цитотоксический эффект.
- Иммунорегулирующие свойства.
- Образование циркулирующих иммунных комплексов (ЦИК).
Структура молекулы иммуноглобулина
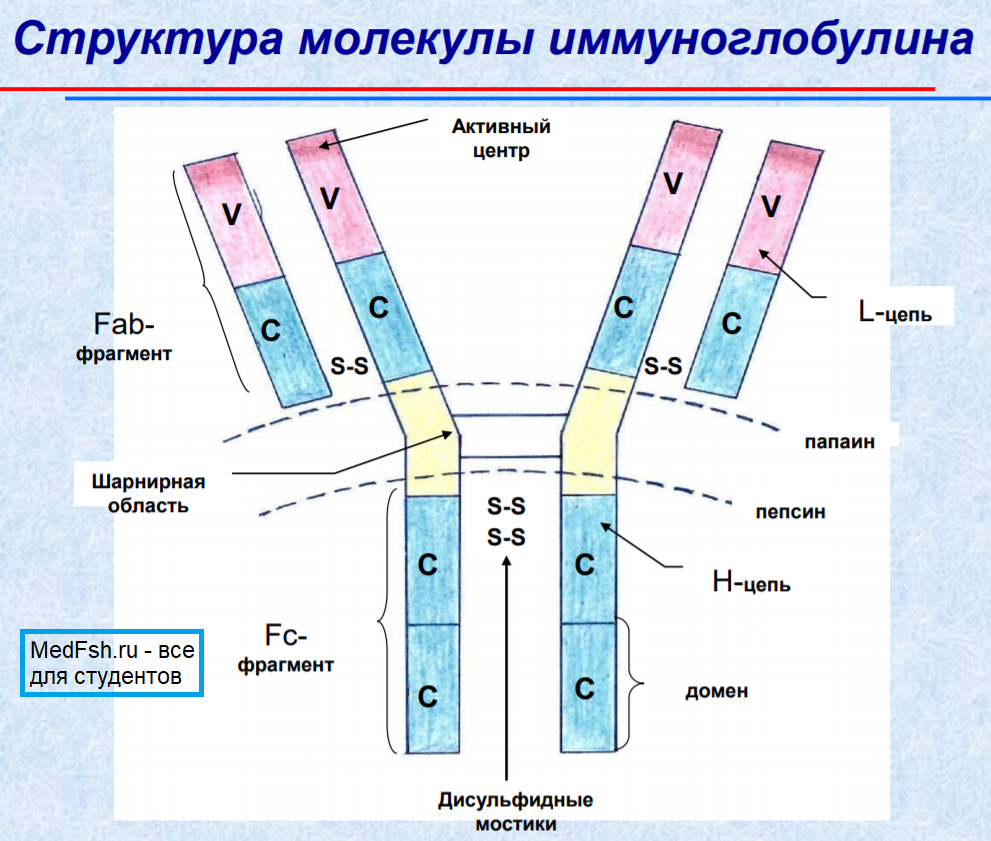
Характеристики иммуноглобулинов:
- Валентность – количество активных (антигенсвязывающих) центров антител. Полные антитела как минимум 2-валентны. Неполные – содержат один антигенсвязывающий центр.
- Аффинность – сродство антигенной детерминанты с активным центром антитела, зависит от степени комплементарности структуры антигенсвязывающего центра и антигенной детерминанты.
- Авидность – скорость и прочность связывания антитела с соответствующим антигеном.
- Разнообразие Ig определяет антигенную специфичность.
3 типа антигенных детерминант:
- Изотипические детерминанты (изотипы) – структуры характерные для индивидуумов одного вида. Гетерогенность изотипов связана со структурными различиями константных участков легких и тяжелых цепей. Эти различия обуславливают деление Ig на классы, подклассы. Н-цепи делятся на 5 классов: μ-мю, γ-гамма, αальфа, δ-дельта, ε-эпсилон; L-цепи делятся на 2 типа: κкаппа, λ-лямбда.
- Аллотипические детерминанты (аллотипы) – структуры, характерные для некоторых индивидуумов внутри вида.
- Идиотипические детерминанты (идиотипы) – структуры, характерные только для определенных Ig одного индивидуума. Определяют специфичность взаимодействия данного иммуноглобулина с определенным антигеном.
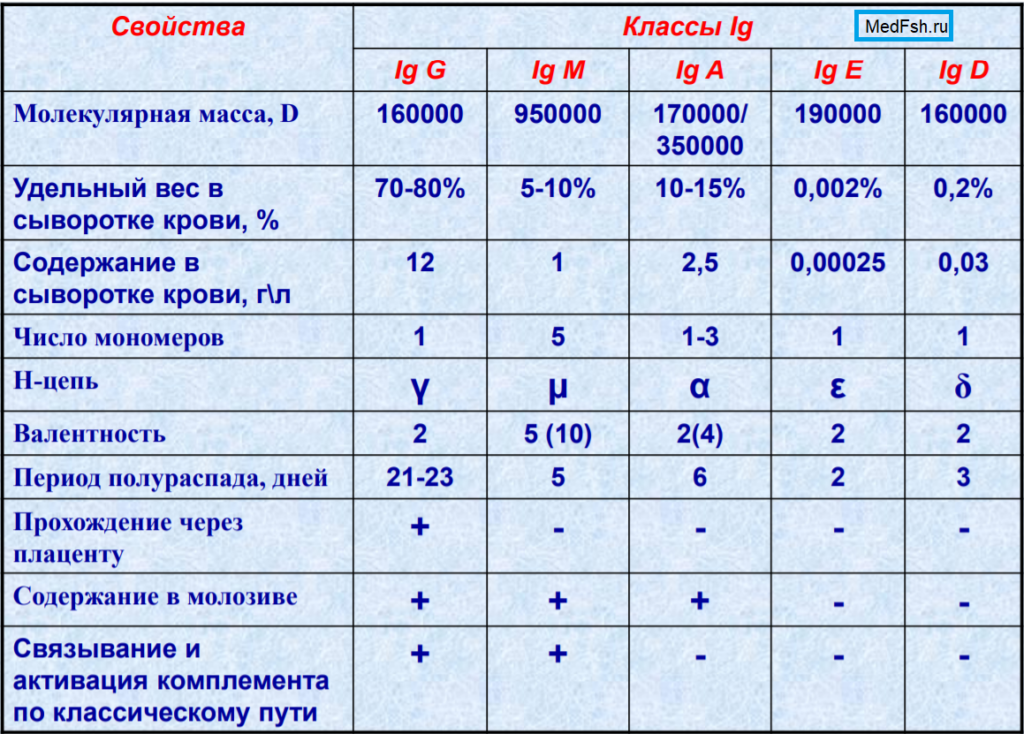
Классы иммуноглобулинов, их свойства и строение
Антитела относятся к γ–глобулиновой фракции белков сыворотки крови. На долю γ–глобулинов приходится 15-25% белков сыворотки крови, и они получили название иммуноглобулинов.
Строение и природа антител
Антитела ― это иммуноглобулины, вырабатываемые в ответ на введение антигена, способные специфически связываться с антигеном и участвовать во многих иммунологических реакциях.рис расположение антигена
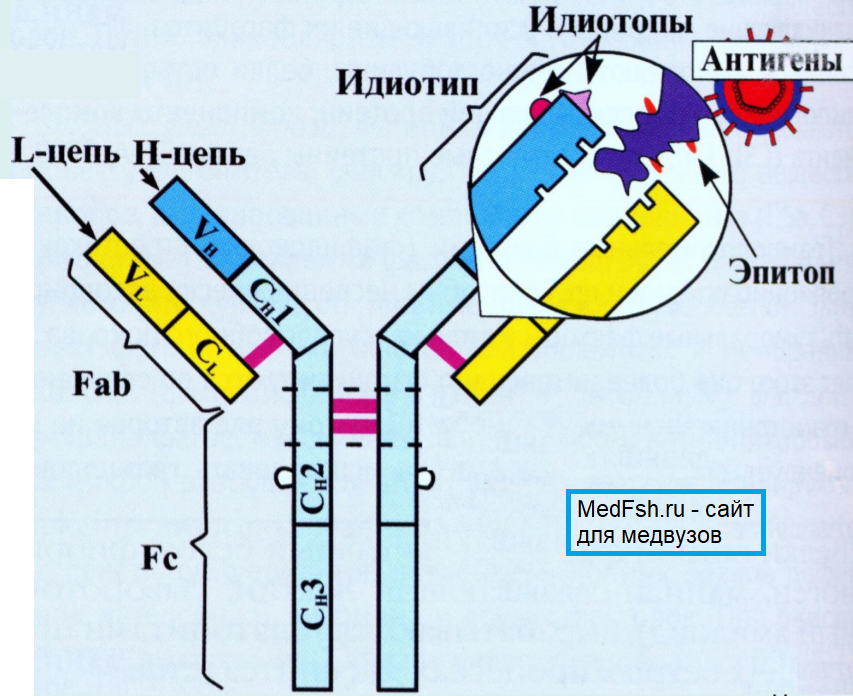
Молекулы иммуноглобулинов всех классов универсальны. Она имеет две полипептидные цепи: 2 ― тяжелые, 2 ― легкие, которые соединены дисульфидными связями.
Иммуноглобулины обладают выраженной специфичностью и подходят к антигенам как ключ к замку, формируя два антигенсвязывающего центра.
Иммуноглобулин класса G
Среди всех классов иммуноглобулинов в количественном отношении доминирует Ig G. В сыворотке млекопитающих он составляет около 75% от общего количества этих белков.
Биологическая роль Ig G разнообразна. Это и антибактериальная защита через механизм комплементзависимого лизиса микробной клетки, и проникновение через плаценту с той же защитной для развивающегося зародыша функцией, и «армирование» макрофагов (цитофильность к макрофагам), в результате чего они становятся цитотоксическими для трансплантатов и опухолей, и участие в повышенной реактивности аллергического типа.
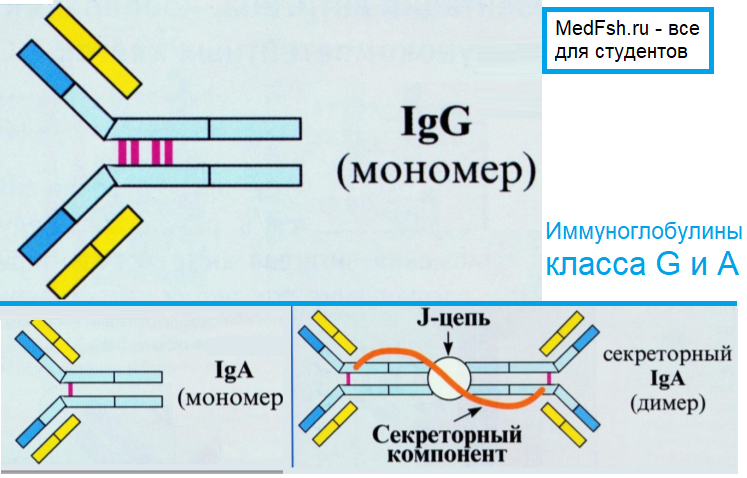
Иммуноглобулин класса А
Имеет две формы:
- сывороточная (циркулирует в виде мономера);
- секреторная (циркулирует в виде димера и обеспечивает местный иммунитет слизистых дыхательных, половых, мочевыделительных путей, ЖКТ).
Является доминирующим иммуноглобулином секретов организма (слюны, пищеварительного сока, выделений слизистой носа и молочной железы). В сыворотке крови его содержание незначительно и составляет всего 10-15% от общего количества всех иммуноглобулинов.
Функционально Ig A выступает в качестве первой линии защиты на слизистых поверхностях, препятствуя проникновению вирусов в организм. Хотя Ig A не связывает комплемент и в силу этого не обладает бактерицидной активностью, он играет важную роль в нейтрализации бактериальных токсинов. Кроме того, у млекопитающих, включая человека, секреторный Ig A хорошо представлен в молозиве и обеспечивает таким образом специфический иммунитет новорожденных.
Иммуноглобулин класса М
Самая крупная молекула из пяти классов. Является пентамером, валентность равна 10. Имеет десять антигенсвязывающих центров. В процессе гуморального иммунного ответа наиболее ранние антитела относятся к Ig М-классу. Они же первыми появляются в онто- и филогенезе. Наибольшую активность Ig М проявляет в антибактериальном иммунитете и при некоторых аутоиммунных заболеваниях.
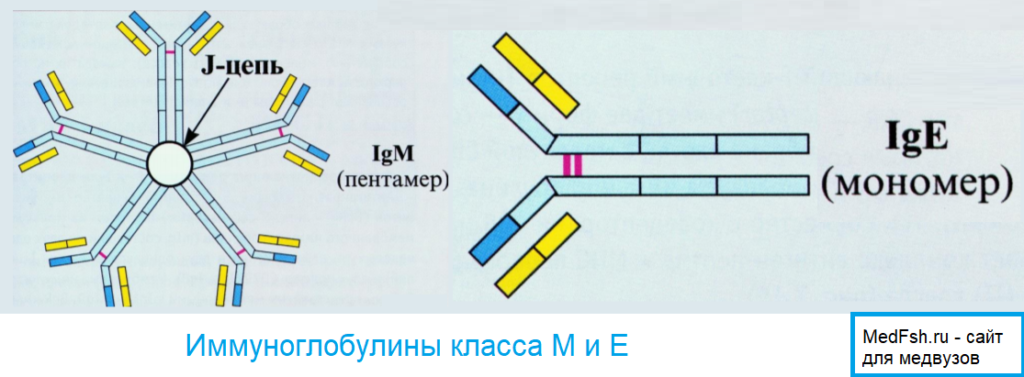
Иммуноглобулин класса Е
Содержание Ig E в сыворотке крайне мало, хотя удельный вес этих иммуноглобулинов в аллергических реакциях является доминирующим.
Функциональная активность Ig E проявляется в развитии аллергических реакций. Данный иммуноглобулин способен взаимодействовать с тучными клетками и базофилами посредством Fc – области и соответствующего рецептора на этих клетках. После связи Ig E с антигеном (аллергеном) тучные клетки получают сигнал к секреции вазоактивных аминов и других фармакологически значимых соединений, что, собственно и приводит к развитию аллергических реакций.
Иммуноглобулин класса D
Иммуноглобулин D был открыт как необычный миеломный белок. Затем его обнаружили в сыворотке крови в очень небольшом количестве.
Данный иммуноглобулин совместно с мономерным Ig М экспрессируется на поверхности В-клеток.
Вопрос о форме участия Ig D в иммунных процессах остается открытым. Содержится в сыворотке крови в очень малых количествах. Известно, что Ig D продуцируют клетками миндалин и аденоидов. Ig D не связывает комплемент, не проходит через плацентарный барьер.
Динамика образования антител при первичном иммунном ответе
Периоды:
- Латентный (3-5 дней) — скрытые процессы восприятия антигенного раздражения, завершаюшиеся поступлением в кровь Ig М.
- Логарифмический (продуктивный) (7-15 дней) — концентрация антител в сыворотке крови резко возрастает — титры Ig M и G достигают максимума.
- Стационарный (максимума и стабилизации) (15-30 дней) — поддерживается максимальный стабильный уровень Ig M и G в крови.
- Снижения (14 дней и более) — концентрация антител в крови постепенно снижается.
Особенности вторичного иммунного ответа:
- Укороченный латентный период (от нескольких часов до 1-2 дней).
- Синтезируются сразу Ig G.
- Более быстрый подъем концентрации антител.
- Большие значения максимальной концентрации антител.
- Высокая скорость образования антител.
- Индукция меньшими дозами антигенов.
Основные типы антител по действию на антиген:
- Антитоксические – нейтрализуют или флоккулируют антигены.
- Агглютинирующие – агрегируют антигены.
- Преципитирующие – образуют комплекс с растворимыми антигенами только в растворах или гелях;
- Лизирующие – вызывают разрушение клетокмишеней.
- Опсонизирующие – взаимодействуют с поверхностными структурами клеток микробов, способствуя поглощению их фагоцитами.
- Нейтрализующие – инактивируют антигены, лишая их возможности проявлять патогенное действие.
Виды антител
- Изоантитела – антитела к изоантигенам. Например, антитела к изоантигенам эритроцитов человека (АВО).
- Нормальные (естественные) антитела – антитела, обнаруживаемые в сыворотке крови без предварительного воздействия антигена. Титры их низкие, а вопрос об их происхождении до конца не решен.
- Аутоантитела – антитела к молекулам веществ, входящих в состав собственных клеток и тканей организма.
- Гетероантитела – антитела, образующиеся в ответ на введение гетероантигена.
- Моноклональные антитела – антитела одной специфичности, синтезируемые искусственно полученным клоном плазмоцитов.
Метод получения моноклональных антител состоит в слиянии сенсибилизированных лимфоцитов с клетками миеломы для получения клеточных гибридов (гибридом). Гибридомы обладают способностью синтезировать антитела и, в то же время, они представляют собой опухолевые клетки, способные к непрерывной пролиферации.
В отличие от поликлональных гетерогенных сывороток, содержащих большое разнообразие антител, отличающихся своей специфичностью, аффинитетом и физикохимическими свойствами, препараты моноклональных антител содержат продукт единственного клона плазматических клеток, направленный к строго определенной антигенной детерминанте и обладающий всегда одинаковыми физико-химическими характеристиками и сродством к антигену.
Получение гибридом включает этапы:
- Получение миеломной линии.
- Получение селезеночных клеток от иммунизированного организма (плазмоциты, синтезирующие Ig определенной специфичности).
- Создание в культуре условий для того, чтобы хотя бы некоторые клетки одной и другой популяции могли слиться.
- Выделение слившихся клеток и накопление их клонов.
- Отбор интересующего клона, его накопление и использование. Накопление клона осуществляют in vitro или путем введения животным.
Использование моноклональные антител:
- идентификация субпопуляций лимфоцитов человека,
- истощение клеточных популяций,
- выделение клеток,
- установление функций молекул клеточной поверхности,
- определение группы крови,
- диагностика опухолей и локализация опухолей,
- иммунорадиометрический анализ,
- анализ сложных смесей антигенов,
- анализ эмбрионального развития,
- анализ иммунного ответа,
- искусственные ферменты.
За последние 15 лет около 30 терапевтических моноклональных антител были утверждены. Большинство из них молекулы IgG1. Некоторые причины успеха этого класса Ig обусловлены тем, что они обладают долгим временем полу-жизни в сыворотке, а также эффекторными функциями их Fc регионов.
Моноклональные антитела химерные — константная часть мышиных антител замещена соответствующей константной областью иммуноглобулина человека и в своей структуре имеют более 65% человеческого иммуноглобулина. Гуманизированные моноклональные антитела – до 95% состоят из человеческого иммуноглобулина. Кроме того, трансгенные технологии (фаговый дисплей) были использованы для создания полностью человеческих моноклональных антител (Fully human monoclonal antibodies)
Моноклональные антитела
Названия всех моноклональных антител оканчиваются на «–mab» (от monoclonal antibody). Если антитело получено от мыши, добавляется буква «о», и окончание у таких антител «-omab». Химерные антитела получили окончание «-ximab». Гуманизированные антитела имеют окончание «-zumab», полностью человеческие – «-umab».
Производство моноклональных антител является наиболее быстро развивающимся сегментом фармацевтической индустрии, составляющим третью часть всех биотехнологических продуктов. По итогам 2010 г. два моноклональных антитела — Rituxan/MabThera и Remicade — вошли в Toп-5 блокбастеров среди биотехнологических препаратов. В 2015 г. все существующие на рынке препараты (60 млрд. долл. ежегодных продаж) утратят патентную защиту, и рынок продаж подобных биотехнологических препаратов значимо увеличится.
Трастузумаб (Trastuzumab, Герцептин)
Трастузумаб (Trastuzumab, Герцептин) – рекомбинантное МкАТ, которое избирательно связывается с рецептором HER2 на поверхности опухолевых клеток многих солидных опухолей. Препарат Herceptin (Trastuzumab) был разработан компанией Genentech и введен в клиническую практику в 1998 году. Применение Герцептина радикально изменило лечение рака молочной железы, в руках онкологов появилось новое эффективное лекарство, позволяющее вылечить или продлить жизни многочисленных пациентов.
Рецептор HER2 — белковая молекула, расположенная на поверхности опухолевых клеток. Примерно в 25 % случаев рака молочной железы злокачественные клетки содержат повышенное количество данных рецепторов (HER2 — позитивный рак молочной железы). При HER2 — позитивном раке молочной железы происходит постоянная стимуляция злокачественного роста за счет присоединения выделяемого самой опухолью вещества, известного как эпидермальный фактор роста, к рецептору HER2. Герцептин блокирует рецептор HER2, что не позволяет эпидермальному фактору роста стимулировать процесс деления злокачественных клеток.
Ритуксимаб (Ритуксан, Мабтера)
Ритуксимаб (Ритуксан, Мабтера) представляет собой химерные моноклональные антитела мыши/человека специфически связывающиеся с CD20+ антигеном. Этот антиген локализуется на поверхности пре-В-лимфоцитов и зрелых B лимфоцитов, но отсутствует на стволовых гемопоэтических клетках, нормальных плазматических клетках и здоровых клетках других тканей. Этот антиген экспрессируется более чем в 90% В-клеточных неходжкинских лимфом. Механизм действия Ритуксана связан с развитием опосредованной антитело–зависимой клеточной и комплемент–зависимой цитотоксичности, что вызывает гибель клеток лимфомы, положительных по CD20. Происходит снижение уровня циркулирующих CD20+ В–лимфоцитов, как лимфомных, так и нормальных.
Ритуксимаб — это химерное моноклональное антитело, имеющее вариабельный мышиный и константный человеческий регион, специфически связанное с антигеном CD20 на В-лимфоцитах и инициирующее иммунологические реакции, которые опосредуют лизис В-клеток. В последние годы препарат зарегистрирован еще для лечения широкого круга аутоиммунных заболеваний с гиперфункцией В-клеток.
Алемтузумаб (Кампат, Кэмпас, Campath)
Еще одним высокоэффективным препаратом для лечения хронического лимфолейкоза (наиболее частого вида лейкоза у взрослых) являются антитела против CD52 антигена. Препарат Алемтузумаб (Кампат, Кэмпас, Campath) – гуманизированное МКА, связывающееся с CD52. Антиген CD52 экспрессируется на мембране большинства зрелых нормальных и опухолевых Т- и В-лимфоцитов с очень высокой плотностью — примерно 500 000 молекул на клетку (по сравнению с антигеном CD20, плотность экспрессии которого составляет около 8000 молекул на клетку). Этим объясняется чрезвычайно высокая активность алемтузумаба в отношении хронического лимфолейкоза и Тклеточных лимфом. Алемтузумаб (Кампат, Кэмпас, Campath)
Важно отметить данный антиген обнаружен на поверхности незначительной части (менее 5%) гранулоцитов и отсутствует на эритроцитах и тромбоцитах. Не повреждает стволовые кроветворные клетки и клеткипредшественники. Другое название препарата Лемтрада (Lemtrada).
В последние годы Кэмпас используется для уменьшения реакции «трансплантат против хозяина» при аллогенной трансплантации стволовых кроветворных клеток (им предварительно очищают трансплантат).
Радиоиммунотоксины на основе анти-CD20 антител
Два препарата на основе МКА к CD20 антигену, меченные радиоактивными изотопами, разрешены к клиническому применению при неходжкинской лимфоме.
Ибритумомаб (ibritumomab, Зевалин) является конъюгатом Мабтеры (МкАТ против CD20) с радиоактивным изотопом иттрия–90 (Y90). Показаниями к использованию Зевалина является рецидивирующая неходжкинская лимфома, в том числе и при прогрессировании после Мабтеры.
Бексар (J131Tositumomab, Bexxar) – конъюгат мышиного МкАТ против CD20 антигена с радиоактивным изотопом йода J131. Период полураспада данного изотопа составляет 8 дней. J 131-тозитумомаб обладает способностью к специфическому связыванию с CD20, тем самым обусловливая лизис клеток, экспрессирующих данный антиген, а также способствует гибели соседних клеток.
Отдельную группу терапевтических моноклональных антител составляют препараты, действие которых направлено на воспалительный процесс. Наиболее важной “мишенью” для “антицитокиновой” терапии МкАТ является “провоспалительный” цитокин – фактор некроза опухоли (ФНО)–α. ФНО-α играет ведущую роль в развитии самых разнообразных проявлений, характерных для многих воспалительных заболеваний человека.
Ремикейд (инфликсимаб) — Infliximab (REMICADE)
Ремикейд (инфликсимаб) представляет собой моноклональные антитела к одному из ключевых цитокинов, вовлеченных в развитие воспалительных процессов, — фактору некроза опухоли (tumor necrosis factor alpha — TNF-alpha). Как полагают исследователи, TNF также играет важную роль не только в развитии ревматоидного артрита, но и псориаза.
Действие Ремикейда, как биологического агента, направлено на ключевую молекулу воспалительных и иммунологических процессов, лежащих в основе ревматоидного артита — на фактор некроза опухоли альфа (ФНО-α ). Доказано, что Ремикейд предотвращает деструкцию суставов. Ремикейд, возможно, первый антиревматический препарат, приостанавливающий прогрессирование заболевания, при этой патологии он в большей степени изучен.